Resumen
Clínica veterinaria: abordaje diagnóstico y terapéutico
ISSN: 2395-8766
Una forma de citar este artículo:
- Bolaños-Aguilar LA, Sánchez-Sánchez T, Martínez-Chavarría LC, Ramos-Garduño LA, Reyes-Matute A, Maldonado-Reséndiz RI. Encefalitozoonosis en un grupo de conejos (Oryctolagus cuniculus) de compañía. Clínica Veterinaria: abordaje diagnóstico y terapéutico. 2019;5:e30201951. doi:10.22201/fmvz.23958766e.201930.
Resumen
Descripción del caso. Dos gazapos en una población de diez conejos de compañía murieron súbitamente y el estudio histopatológico reveló que tenían lesiones compatibles con encefalitozoonosis (uveítis facoclástica, encefalitis piogranulomatosa con esporas y pseudoquistes compatibles con E. cuniculi). El resto de la población (ocho conejos) se presentó en el Hospital Veterinario de Especialidades en Fauna Silvestre y Etología Clínica (HVE-FSEC) de la Facultad de Medicina Veterinaria y Zootecnia de la UNAM para ser evaluados clínicamente.
Tratamiento y evolución No hay tratamiento curativo para E. cuniculi y es una zoonosis. En la familia de los propietarios, había dos adultos mayores, personas con mayor riesgo potencial, por lo que se recomendó confinar a la población de conejos de compañía en un lugar aislado y minimizar la exposición. Por razones económicas los propietarios no podían mantener a los conejos en confinamiento, así que se les propuso aplicar la eutanasia a los ocho individuos; ellos estuvieron de acuerdo.
Pruebas de laboratorio. Se realizó el estudio histopatológico que incluyó tinciones de rutina y tinciones especiales. Además, a partir de los bloques de parafina que contenían fragmentos de los órganos con las principales lesiones (cerebro y riñón), se extrajo ADN para realizar la prueba de reacción en cadena de la polimerasa (PCR) anidada. El resultado fue positivo para este microorganismo, ya que se amplificó el fragmento de 549 pb del gen 16S específico de E. cuniculi.
Relevancia clínica. En este artículo se reporta por primera vez la presencia de E. cuniculi en una población de conejos de compañía en México. La prueba confirmatoria es la reacción en cadena de la polimerasa anidada. La encefalitozoonosis es una enfermedad zoonótica, que tiene alta seroprevalencia en las poblaciones de conejos a nivel mundial, sin embargo es una enfermedad altamente subdiagnosticada. El diagnóstico es difícil de realizarse in vivo, sin embargo, se puede realizar la PCR como prueba confirmatoria del patógeno. Es necesario establecer medidas de bioseguridad por su potencial zoonótico, así como seguir generando información epidemiológica para mejorar la sanidad animal y la salud pública.
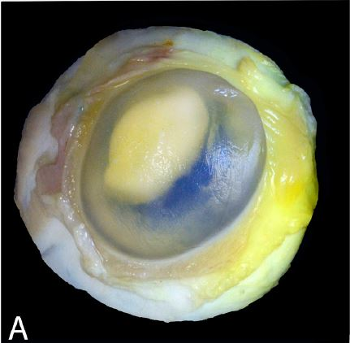
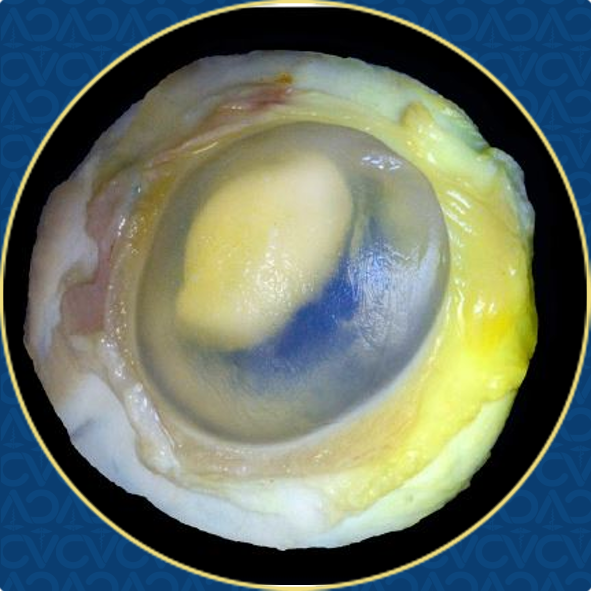
Figura 1 A) Globo ocular de gazapo 2 con uveítis, en el cual se observa un material blanco-amarillento que ocupa el 60 % de la cámara anterior del ojo.
Encephalitozoonosis in a group of pet rabbits (Oryctolagus cuniculus)
Abstract
Case description. Two young rabbits in a population of ten pet rabbits died suddenly and the histopathological study revealed that they had compatible lesions with encephalitozoonosis (phacoclastic uveitis, pyogranulomatous encephalitis with spores and pseudocysts compatible with E. cuniculi). The rest of the population (eight rabbits) was presented at the Hospital Veterinario de Especialidades en Fauna Silvestre y Etología Clínica (HVE-FSEC) of the Facultad de Medicina Veterinaria y Zootecnia of the UNAM to be evaluated clinically.
Treatment and evolution. There is no curative treatment for E. cuniculi and it is a zoonosis. In the owners' family, there were two older adults, people at higher potential risk, so it was recommended to confine the pet rabbit population to an isolated location and minimize exposure. For economic reasons the owners could not keep the rabbits in confinement, so they were proposed to euthanize the eight individuals; they agreed.
Laboratory tests. The histopathological study was performed which included routine stains and special stains. In addition, from paraffin blocks containing fragments of the organs with the main lesions (brain and kidney), DNA was extracted to perform the nested polymerase chain reaction (PCR). The result was positive for this microorganism, as the 549 pb fragment of the 16S gene specific to E. cuniculi was amplified.
Clinical relevance. This article reports for the first time the presence of E. cuniculi in a population of companion rabbits in Mexico. The confirmatory test is the chain reaction of the nested polymerase. Encephalophozoonosis is a zoonotic disease, which has high seroprevalence in rabbit populations worldwide, but is a highly underdiagnosed disease. The diagnosis is difficult to make in vivo, however, PCR may be performed as a confirmatory pathogen test. It is necessary to establish biosafety measures for their zoonotic potential, as well as to continue generating epidemiological information to improve animal health and public health.
Keywords: Encephalitozoon cuniculi, rabbits, Oryctolagus cuniculus, phacoclastic uveitis, interstitial nephritis, pyogranulomatous encephalitis, zoonosis.
Referencias
Csokai J, Joachim A, Gruber A, Künzel F, Ticky A. Diagnostic markers for encephalitozoonosis in pet rabbits. Vet Parasit 2009:163:18ꟷ26. doi: 10.1016/j.vetpar.2009.03.057.
Thomarat F, Vivarès CP, Gouy M. Phylogenetic analysis of the complete genome sequence of Encephalitzoon cuniculi supports the fungal origen of Microsporidia and reveals a high frequency of fast-evolving genes. J Mol Evol. 2004;59:790. doi: 10.1007/s00239-004-2673-0.
Künzel F, Fisher P G. Clinical signs, diagnosis and treatment of Encephalitozoon cuniculi infection in rabbits. Vet Clin Exot Ani. 2018;21:69ꟷ82. doi: 10.1016/j.cvex.2017.08.002.
Castañón-Olivares LR, Pineda-Murillo J. Microsporidiosis. 2014 (consultado 7 julio 2018) Disponible en: http://www.facmed.unam.mx/deptos/microbiologia/micologia/microsporidiosis.htm
Didrer ES, Stovall ME, Green LC, Brindley PJ, Sestak K, Didier OJ. Epidemiology of microsporidiosis: sources and modes of transmission. Vet Parasitol. 2004;126:145ꟷ166. doi: 10.1016/j.vetpar.2004.09.006.
Maddox JV, Brooks WM, Solter LF. Bioassays of microsporidia. En: Navon A, Ascher KRS, editores. Bioassays of entomopathogenic microbes and nematodes. New York, NY US: CABI Publishing, 2011.
Felchle LM, Sigler RL. Phacoemulsification for the management of Encephalitozoon cuniculi-induced phacoclastic uveitis in a rabbit. Veterinary Ophtalmology. 2002;5(3):211ꟷ215. doi: 10.1046/j.1463-5224.2002.00240.x.
Maestrini G, Ricci E, Cantile C, Mannella R, Mancianti F, Paci G, D´Ascenzi, Perrucci S. Encephalitozoon cuniculi in rabbits: Serological screening and histopathological findings. Comp immunol Microb Infect Dis 2017;50:54ꟷ57. doi: 10.1016/j.cimid.2016.11.012.
Desoubeaux G, Patin A, Pesechke R, Joachim A, Cray C. Application of Western blot analysis for the diagnosis of Encephalitozoon cunculi infection in rabbits; example of a quantitative approach. Parasitol Res. 2017;116(2):743ꟷ750. doi: 10.1007/s00436-016-5343-4.
Furuya K, Asakura T, Igarashi M et al. Microsporidian Encephalitozoon cuniculi antibodies in rabbit urine samples. Vet Rec. 2009;165(3):85ꟷ86. doi: 10.1136/vetrec.165.3.85.
Csokai J, Gruber A, Künzel F, Ticky A, Joachim A. Encephalitozoonosis in pet rabbits (Oryctolagus cuniculus): pathohistological findings in animals with latent infection versus clinical manifestation. Parasitol Res. 2009;104(3):629ꟷ635. doi: 10.1007/s00436-008-1239-2.
Rodriguez-Tovar LE, Nevárez-Garza AM, Trejo-Chávez A, et al., Encephalitozoon cuniculi: grading the histological lesions in brain, kidney and liver during primoinfection outbreak in rabbits. J Pathog. 2016:1ꟷ9. doi: 10.1155/2016/5768428.
Katzwinkel-Wladarsch D, Deplazes P, Weber R. Comparison of polymerase chain reaction with light microscopy for detection of microsporidia in clinical specimens. Eur J Clin Microbiol Infect Dis. 1997;16:7ꟷ10. doi: 10.1007/BF01575111.
Abu-Akkada SS, Oda SS. Prevention and treatment of Encephalitozoon cuniculi infection in immunosuppressed rabbits with fenbendazole. Iran J Vet Res. 2016;12(2):98ꟷ105.
Suter C, Müller-Doblies UU, Hatt JM. Prevention and treatment of Encephalitozoon cuniculi infection in rabbits with fenbendazole. Vet Rec. 2001;148:478ꟷ80. doi: 10.1136/vr.148.15.478.
Ozcan O, Ozcan AT., Zafer K. Encephalitozoonosis in New Zealand rabbits and potential transmission risk. Vet parasitol. 2011;179(1ꟷ3):234ꟷ7. doi: 10.1016/j.vetpar.2011.02.007.
Weber R, Deplazes P, Flepp M, Mathis A, Baumann R, Sauer B, Kuster H, Lüthy R. Cerebral Microsporidiosis due to Encephalitozoon cuniculi in a patient with human immunodeficiency virus infection. N Engl J Med. 1997;336(7):474ꟷ478. doi: 10.1056/NEJM199702133360704.
Chilón CVJ. Seroprevalencia de Encephalitozoon cuniculi en conejos destinados como mascotas en la provincia de Lima. (tesis de licenciatura) Perú. Universidad Nacional Mayor de San Marcos; 2014.
Waller T. Sensitivity of Encephalitozoon cuniculi to various temperatures, disinfectants, and drugs. Lab Animals. 1979;13:227ꟷ230. doi: 10.1258/002367779780937753.